Cours de soutien scolaire physique chimie en ligne spécial première et terminale S ou STL, avec cette fiche méthode sur le tableau d’avancement.
Karine vous propose ce second cours de physique chimie en ligne destinée à votre révision du bac. Un premier article présentait une fiche méthode sur le tableau d’avancement. Après le cas général, voyons aujourd’hui le CAS n°1 :
Le dioxygène O2 est le réactif LIMITANT
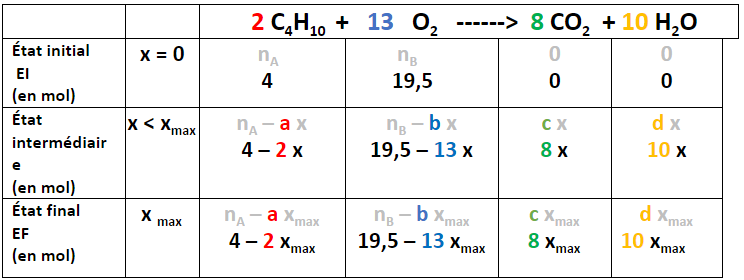
On fait réagir 4 moles de butane C4H10 (nA = 4) avec 19,5 moles de dioxygène O2 (nB = 19,5)
En remplaçant a, b, c et d par les coefficients stœchiométriques de l’équation bilan 2 ; 13 ; 8 et 10
L’avancement maximal xmax est obtenu quand l’un des réactifs a été totalement consommé.
Déterminer xmax revient à résoudre
4 – 2 xmax = 0 ↔ xmax = 4/2 = 2 mol
et 19,5 – 13 xmax = 0 ↔ xmax = 19,513 = 1,5 mol
On choisit la plus petite valeur de xmax , ici xmax = 1,5 mol. Le réactif limitant est donc le dioxygène O2.
On remplace la valeur de Xmax dans la dernière ligne afin d’obtenir le bilan à la fin de la réaction à savoir le reste des réactifs et des quantités de produits formés
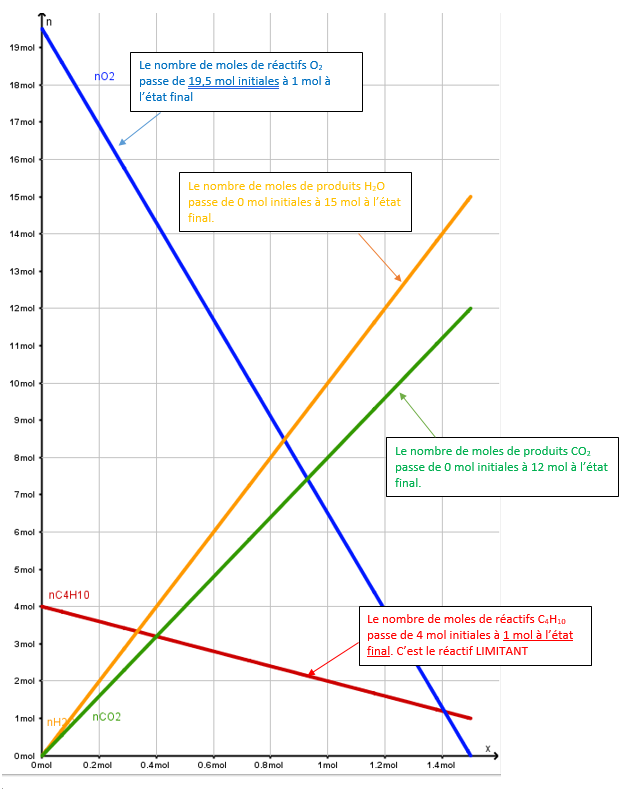
À l’aide du logiciel Geogebra, on peut tracer les courbes d’évolution des quantités de réactifs et de produits en fonction de l’avancement:
Quiz récapitulatif sur le tableau d’avancement |
| À vous maintenant ! On fait réagir 5 moles de butane C4H10 et avec 39 moles de dioxygène O2 |
| 2 C4H10 + 13 O2 ——-> 8 CO2 + 10 H2O |
1/ Quel est le réactif limitant ?
|
2/ Quelle est la valeur de l’avancement maximal xmax ?
|
3/ À la fin de la réaction, quel est le nombre de moles de dioxygène O2 restant ?
|
4/ Quel est le nombre de moles de dioxyde de carbone CO2 produit ?
|
5/ Quel est le nombre de moles d’eau formé ?
|
Bon courage.
RÉPONSES :
- a) le butane C4H10
- b) 2,5 mol
- c) 6,5 mol
- b) 20 mol
- a) 25 mol




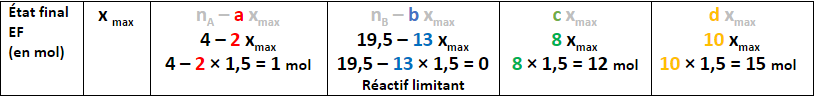


Répondre
Want to join the discussion?Feel free to contribute!